Sách giáo khoa và đề thi môn hóa sẽ phải được viết lại sau khám phá này: Carbon bây giờ đã có thể liên kết với Carbon bằng 1 electron duy nhất!
Hãy nhớ lại một chút kiến thức về môn hóa học thời phổ thông: Khi viết công thức của những hợp chất hữu cơ, bạn thường viết liên kết giữa Carbon và Carbon như thế nào?
Có phải bạn sẽ viết một chữ C, nối với một chữ C bằng dấu gạch ngang (C-C) hay không? Tương tự với các liên kết C=C và C≡C, trong đó, mỗi dấu gạch ngang biểu thị cho một cặp electron, nghĩa là 2 electron, tạo nên liên kết cộng hóa trị.
Suốt thời trung học, chúng ta đã được dạy rằng một nguyên tử Carbon chỉ có thể liên kết với một nguyên tử Carbon khác thông qua 6, 4 hoặc 2 electron. Không có chuyện C liên kết với C chỉ bằng 1 electron duy nhất. Nhưng bây giờ, điều đó đã thực sự xảy ra.
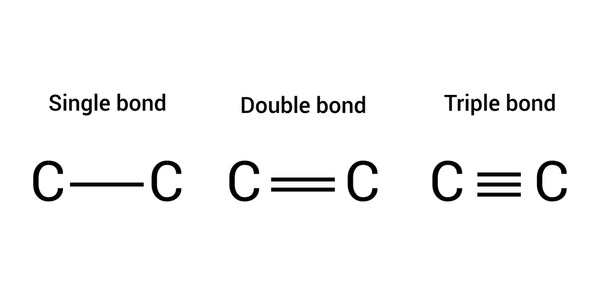
Sách giáo khoa hóa học ngày nay cho rằng mỗi dấu gạch ngang biểu thị cho một cặp electron, nghĩa là 2 electron, tạo nên liên kết cộng hóa trị. Không thể có dạng liên kết C.C với một electron duy nhất.
Trong một nghiên cứu mới trên tạp chí Nature, một nhóm các nhà khoa học Nhật Bản cho biết họ đã tìm thấy bằng chứng đầu tiên cho một liên kết đơn electron có thể xảy ra giữa hai nguyên tử Carbon.
Điều này sẽ khiến định nghĩa liên kết cộng hóa trị phải được viết lại, và "nó sẽ sớm có trong sách giáo khoa của bạn", bài báo trên Nature cho biết.
Xin chia buồn với các sĩ tử tham gia kỳ thi tốt nghiệp THPT quốc gia năm sau, bởi kể từ giờ phút này, với sự xuất hiện của các liên kết C.C bên cạnh C-C đề thi của các bạn chắc chắn sẽ phức tạp hơn đôi chút.
Dự báo của Pauling năm 1931 đã trở thành hiện thực
Bất kể ai từng học hóa đều biết Carbon là một trong những nguyên tố phổ biến nhất trên Trái Đất. Các dạng liên kết và thù hình mà Carbon có thể cấu thành với chính nó cũng đa dạng hơn bất kỳ nguyên tố nào có mặt trong vũ trụ.
Chẳng hạn, Carbon có thể tự mình tạo thành các chuỗi dài một chiều, hoặc tạo thành các cấu trúc đơn nguyên tử sắp xếp theo hình lục giác, thứ mà chúng ta gọi là graphene. Xếp chồng nhiều lớp graphene lên nhau, bạn sẽ được than chì.
Và nếu một nguyên tử Carbon liên kết với 4 nguyên tử Carbon khác bằng các dấu gạch nối biểu thị cho liên kết cộng hóa trị, nó sẽ tạo thành kim cương.
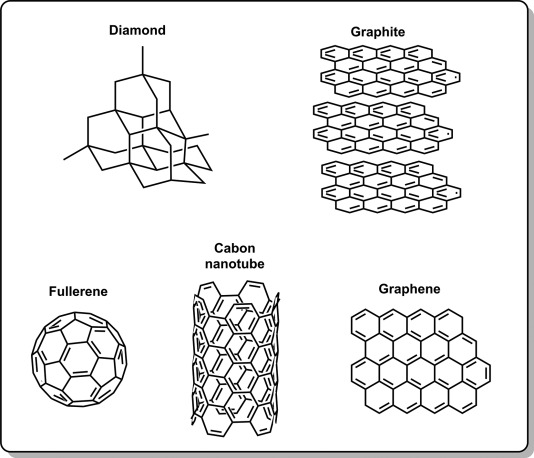

Các dạng thù hình đa dạng của carbon
Nhưng mọi chuyện thậm chí chưa dừng lại ở đó. Gần đây, các nhà khoa học cho biết một nguyên tử Carbon thậm chí có thể liên kết với chính nó, tạo ra một loại "Carbon xanh". Và một dạng thù hình liên quan đến 60 nguyên tử Carbon kết hợp lại với nhau tạo thành một "quả bóng" siêu bền vững gọi là "buckyball".
Đó là chưa kể đến vô số các dạng thù hình có được khi các nguyên tử Carbon sắp xếp ngẫu nhiên, gọi là Carbon vô định hình. Tổng kết lại, chỉ riêng Carbon đã sở hữu hơn 10 dạng thù hình đặc trưng khác nhau, so với chỉ 2-3 dạng thù hình của các nguyên tố phổ biến như Oxy, Nitơ và Phosphor.
Nhưng dù ở bất cứ dạng thù hình nào, các liên kết cộng hóa trị của Carbon cũng phải tuân thủ theo một nguyên tắc, chúng phải trao đổi số lượng electron chẵn để bắt cặp với nhau:
Nếu hai nguyên tử C chia sẻ 1 cặp electron, nó gọi là liên kết đơn: C-C.
Nếu hai nguyên tử C chia sẻ 2 cặp electron, nó gọi là liên kết đôi: C=C.
Nếu hai nguyên tử C chia sẻ 3 cặp electron, nó gọi là liên kết ba: C≡C.
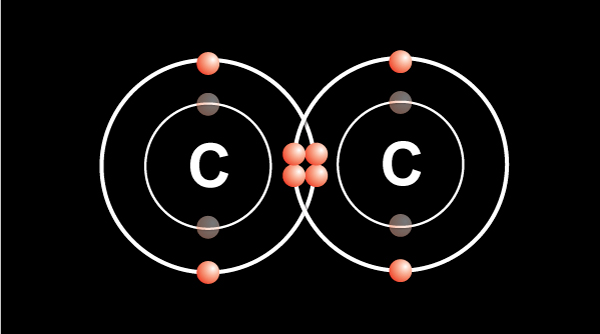
Hai nguyên tử carbon dùng chung 2 cặp electron, tạo thành liên kết đôi C=C.
Định nghĩa liên kết cộng hóa trị cho rằng hai nguyên tử phải dùng chung các cặp electron nghĩa là không thể có một electron đứng đơn lẻ trong liên kết: C.C.
Nhưng vào năm 1931, nhà hóa học đại tài Linus Pauling từng dự đoán rằng biết đâu, một liên kết C.C có thể tồn tại trong một số hợp chất nhất định.
"Những liên kết này không điển hình bằng liên kết cặp electron, vì chúng chỉ xuất hiện trong một số ít hợp chất, tuy nhiên, chúng lại đặc biệt thú vị vì các đặc tính bất thường và khó hiểu của chúng", ông viết trong một bài báo đăng trên Tạp chí của Hiệp hội Hóa học Hoa Kỳ.
Pauling sau đó đã giành giải Nobel Hóa học vào năm 1954 "cho nghiên cứu của ông về bản chất của liên kết hóa học và ứng dụng của nó để làm sáng tỏ cấu trúc của các chất phức tạp". Nhưng phải đến tận bây giờ, gần 100 năm sau bài báo năm 1931 của Pauling, dự đoán của ông mới trở thành hiện thực.
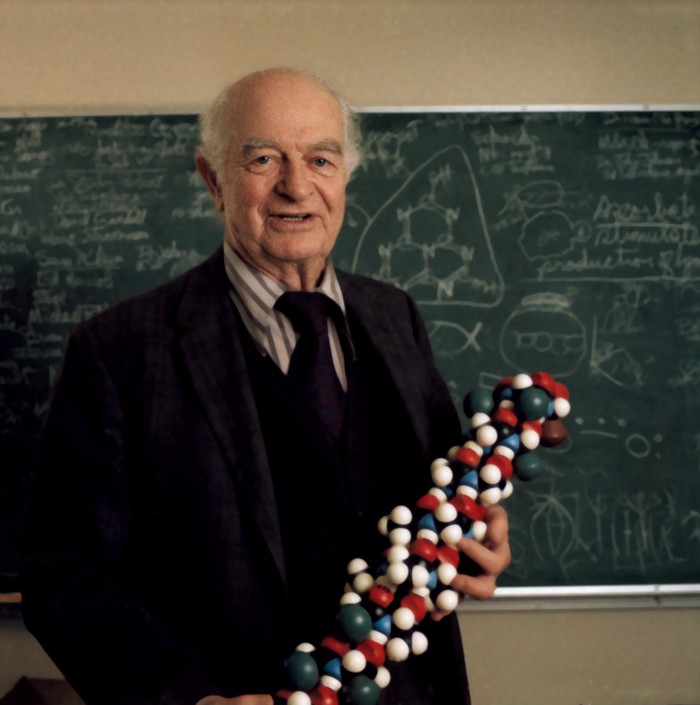
Nhà hóa học đại tài Linus Pauling từng dự đoán về sự tồn tại của liên kết C.C.
Carbon có thể liên kết với Carbon bằng 1 electron duy nhất
Trong một nghiên cứu mang tính đột phá vừa đăng trên tạp chí Nature, bốn nhà khoa học đến từ Đại học Hokkaido ở Nhật Bản đã thực hiện thành công một thí nghiệm để chứng minh dự đoán của Pauling là thật. Họ đã tạo được ra hai nguyên tử Carbon liên kết với nhau chỉ bằng một electron duy nhất.
Cụ thể, các nhà khoa học đã sử dụng dẫn xuất của một hợp chất Carbon gọi là hexaphenylethane để giúp cấu trúc thí nghiệm của họ. Phân tử hexaphenylethane sau đó bị phân hủy dần dần từ trong ra ngoài để lại một "lớp vỏ" mà ở đó, hai nguyên tử Carbon có thể sắp xếp lỏng lẻo, không cần phải tự giữ chặt với nhau.
Tại khoảnh khắc này, các nhà nghiên cứu đã sử dụng một kỹ thuật tia X chuyên dụng để quan sát các liên kết giữa Carbon và Carbon thu được. Các ảnh chụp từ kỹ thuật tia X đã xác nhận các liên kết này chỉ có một electron duy nhất:
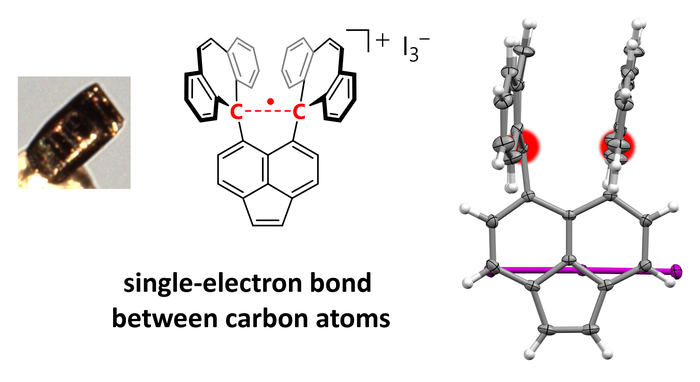
Liên kết đơn electron giữa hai nguyên tử Carbon đã được quan sát thấy trong mảnh vật liệu này.
Nếu hình dung một liên kết đơn C-C, có hai electron bắt cặp với nhau là một cái bắt tay, trong đó hai người đều nắm chặt cổ tay người đối diện, thì liên kết đơn electron C.C giống như một cái bắt tay bình thường giữa hai người.
Nó không quá yếu nhưng cũng không mạnh bằng liên kết cộng hóa trị thường thấy.
"Chúng tôi muốn làm rõ liên kết cộng hóa trị là gì-cụ thể là, tại thời điểm nào một liên kết được coi là cộng hóa trị và tại thời điểm nào thì không?", tiến sĩ Takuya Shimajiri, một trong số các tác giả nghiên cứu tại Đại học Hokkaido cho biết.
Nghiên cứu này chắc chắn sẽ khiến các định nghĩa về liên kết cộng hóa trị từ trước đến nay phải được viết lại. Và nó sẽ sớm có trong sách giáo khoa mới của bạn.

Nếu hình dung một liên kết đơn C-C, có hai electron bắt cặp với nhau là một cái bắt tay, trong đó hai người đều nắm chặt cổ tay người đối diện...

...thì liên kết đơn electron C.C giống như một cái bắt tay bình thường giữa hai người.
Có thể thấy, khám phá mới một lần nữa làm nổi bật tầm nhìn thiên tài của Linus Pauling. Quay trở lại thập niên 1930, trong thời đại của ông, người ta mới chỉ biết tới sự tồn tại của electron trong vài thập kỷ, và lý thuyết về lưỡng tính sóng hạt của nó thậm chí mới ra đời được 6 năm.
Khi Linus Pauling viết về mối liên kết này vào năm 1931, ông nghĩ rằng nó đã tồn tại về mặt lý thuyết và có thể tìm thấy được. Pauling sống thêm 53 năm nữa-trong thời gian đó ông đã giành được hai giải Nobel, một cho Hóa học (năm 1954) và một một Giải Nobel Hòa bình (năm 1962).
Đáng tiếc là Pauling đã không thể đợi đến ngày mà dự đoán của ông trở thành hiện thực. Mặc dù vậy, khi ở trên Thiên Đàng, có lẽ nhà hóa học người Mỹ cũng rất vui mừng khi các nhà khoa học hậu bối của mình cuối cùng cũng cô lập và quan sát được liên kết đơn electron giữa các nguyên tử Carbon.
Với việc viết lại cả định nghĩa của liên kết cộng hóa trị, tầm ảnh hưởng của phát hiện này là rất lớn. Bên cạnh các ứng dụng khác của Carbon như vật liệu nano, graphene ở dạng tấm và dạng ống, có thể phải mất thêm 100 năm nữa mới đi được vào đời sống.
Tất cả cho thấy tầm quan trọng của nguyên tố đứng thứ 6 trong bảng tuần hoàn - Carbon - là không thể phủ nhận.
Nguồn: Nature, Popularmechanics, Pubmed
Thanh Long
Nguồn Phụ Nữ VN : https://phunuvietnam.vn/sach-giao-khoa-va-de-thi-mon-hoa-se-phai-duoc-viet-lai-sau-kham-pha-nay-carbon-bay-gio-da-co-the-lien-ket-voi-carbon-bang-1-electron-duy-nhat-20241016214814611.htm
Tin khác

Câu chuyện về anh chàng Duncan sống ở 25.000 năm trước

4 giờ trước

Cô gái tình cờ phát hiện kho báu quý hiếm hàng nghìn năm tuổi khiến các nhà khoa học cũng phải choáng

4 giờ trước

Những vật liệu đắt nhất thế giới: Top 1 giá trị lên tới tỷ tỷ đô/ounce

4 giờ trước

Quả dứa đắt nhất hành tinh giá 350 triệu đồng, tỷ phú phải xếp hàng mới được mua: Nghe lý do nhiều người không dám tin, bổ ra ăn hương vị càng ngỡ ngàng

23 phút trước

Bí ẩn về loài Tuatara: Chứng nhân sống sót từ thời kỳ khủng long sở hữu 'con mắt thứ ba'

43 phút trước

Top những viên thiên thạch đắt nhất thế giới, nếu nhìn thấy phải nhặt ngay

một giờ trước
